
에폭시 수지는 1개의 분자내 2개 이상의 에폭시기를 갖는 올리고머상의 화합물을 말합니다. 이 에폭시 수지에 에폭시기의 중합을 위한 촉매 또는 경화제를 혼합하여 최종적으로는 열경화성 수지로서 사용됩니다. 에폭시 수지의 경화제로는 에폭시기의 개환부가 반응할 수 있는 1급, 2급 아민류 또는 산무수물 등이 사용됩니다. 에폭시 수지를 성형하는 과정에서 에폭시 수지와 촉매 또는 경화제의 비율을 적절히 조합함에 따라 경화 공정이나 최종 에폭시 수지 경화물의 물성을 조정하는 것이 가능합니다.
에폭시 수지의 종류와 특성
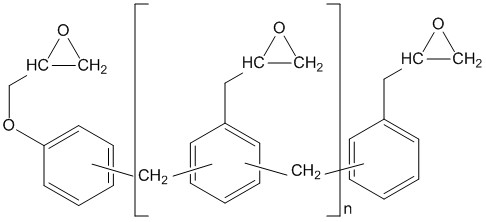
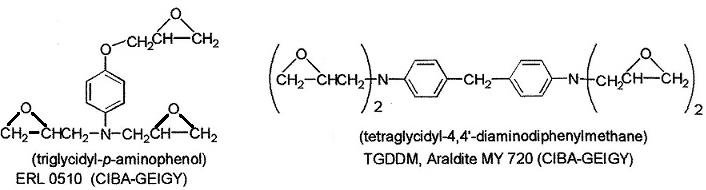
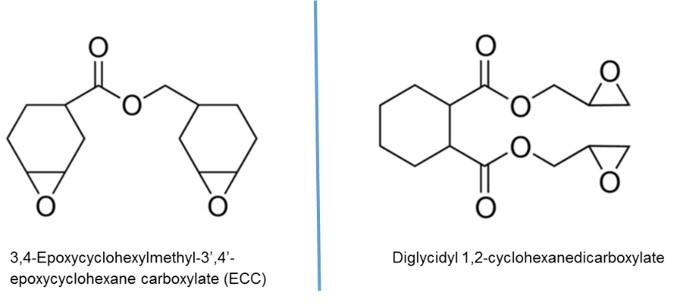
대표적인 에폭시 수지로서는 아래의 그림 1에 나타낸 바와 같은 비스페놀형, 노볼락형, 방향족 아민형, 지환형(고리모양으로 결합된 유기화합물 중 방향족이 아닌)등이 있습니다.
비스페놀 A형 에폭시 수지는 고성능 복합재료의 매트릭스 수지로서 가장 널리 사용되고 있는 물질입니다. 반복 단위 수 n=0의 수지는 상온에서 액상이지만, n=2 정도 이상에서는 고상형으로 됩니다. n값이 증가함에 따라 단위 에폭시기 당의 분자량(에폭시 당량)이 크게 되며, 에폭시기의 반응에 의해 달성 가능한 최대 가교밀도가 낮아지는 특성이 있습니다. 이 때문에 에폭시 당량이 큰 수지에서 얻어지는 경화물은 높은 인성을 나타내지만, 내열성은 저하되는 경향이 있습니다. 복합재료의 매트릭스 수지로 사용되는 에폭시 수지의 경우 n값이 약 0.1 ~ 0.2의 에폭시 수지가 사용되는 것이 일반적입니다.
노볼락형의 에폭시 수지는 2개 이상의 에폭시기를 갖고 분자량이 증가함에 따라 액상에서 고상으로 되지만 경화 후의 노볼락형 수지의 내열성은 분자량에 따라 거의 변화하지 않는 특징이 있습니다.
방향족 아민형의 에폭시 수지는 3 이상의 에폭시기를 가지고 있는데, 질소를 포함하고 있기 때문에 노볼락형에 비교해서 흡습성이 높다는 특징이 있습니다. 비교적 점도가 낮은 액상으로 존재하고 반응기가 여러 개 있기 때문에 가교밀도가 높은 경화수지가 얻어지고, 이 때문에 내열성을 요구하는 복합재료용 프리프레그의 수지로서 널리 사용됩니다.
그림 1 대표적인 에폭시 수지

경화제와 촉매의 종류와 특징
아민계의 경화제에는 그림 2에 나타낸 바와 같은 지방족계 아민 경화제와 방향족계 아민 경화제로 나눌 수 있습니다. 지방족계 경화제는 방향족계 경화제 대비 아민의 염기성이 높기 때문에 경화 속도가 빠르고 실온에서도 경화가 잘 된다는 장점이 있습니다. 그러나 공기 중에서 이산화탄소를 흡수하기 쉽고, 또한 경화제 자체의 독성이 높아 취급 시 유의해야 하며 이러한 단점을 피하기 위해 아민계 경화제를 산과 화합물로 만들어 사용하는 경우도 있습니다.
일반적으로 방향족계 경화제는 고온 경화용으로 사용되기 때문에 지방족계 경화제보다 내열성이 높은 에폭시 수지를 형성시켜 주는데, 액상이 아니라 고상으로 존재하는 경우가 많기 때문에 에폭시 수지에 균일하게 혼합하는 작업이 추가적으로 필요합니다. 수지에 균일하게 혼합하기 위해 두 종류의 아민계 경화제를 사용하고 융점이 낮은 공융 조성물을 만들어 사용하기도 합니다.
방향족계 경화제는 아민의 홀전자가 방향족 고리와 작용하기 때문에 염기성이 상대적으로 낮습니다. 황을 포함한 DDS(diamino diphynyl sulfone)가 가장 대표적인 예로, DDS를 경화제로서 사용한 에폭시 수지는 비교적 고온, 장시간의 경화조건을 요구하지만 저장 안정성은 높은 물질입니다. 이러한 이유로 DDS는 프리프레그를 제조하기 위한 경화제로서 잘 사용됩니다.
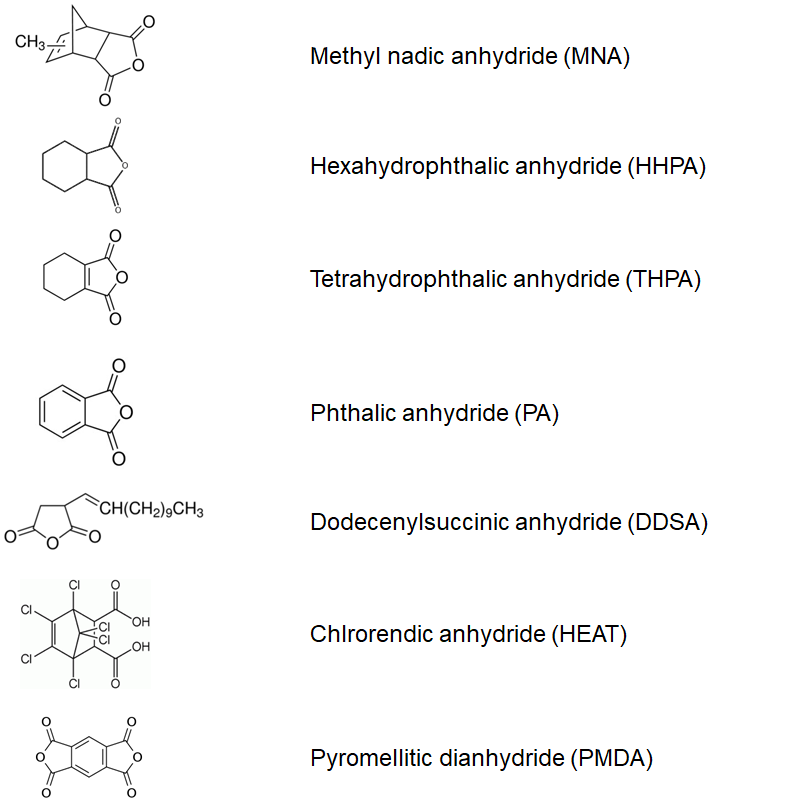
산무수물계 경화제는 촉매가 존재하지 않는 조건에서 아민계 경화제보다도 비교적 반응이 늦어 고온 장시간의 경화조건이 필요합니다. 하지만 경화물의 기계적 성질이 우수하며 발열반응을 최소화하며 경화시킬 수 있기 때문에 filament winding용 수지의 경화제로서 잘 사용됩니다.
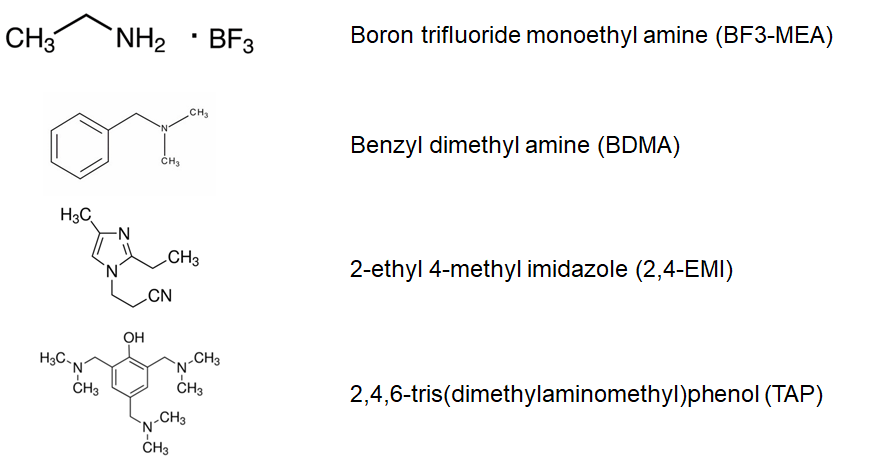
촉매로서는 그림 4에 나타낸 바와 같은 루이스(Lewis) 산형과 루이스(Lewis) 염기형의 화합물이 대표적입니다. 이들 중에서도 루이스(Lewis) 산형의 3불화 붕소 monoethylamine은 단독 중합촉매로서 잘 사용되는 촉매입니다. 루이스(Lewis) 염기형의 촉매용 화합물로는 3급 아민이나 imidazole 화합물이 단독 중합용 촉매 또는 산무수물의 경화 촉진용 촉매로서 널리 사용됩니다.

경화반응과 반응기구
에폭시 수지의 경화의 과정에서 발생하는 화학적 반응은 경화제 및 촉매의 종류에 따라서 다르지만, 모두 공통적으로 에폭시기의 개환 반응으로 출발합니다. 친전자체(Electrophile)에 대해서는 에폭시기 산소의 전자대의 배위가, 친핵체(nucleophile)에 대해서는 탄소-산소간의 분극에 의해서 전자분포가 적어진 탄소원자가 공격을 받아 반응이 시작됩니다. 두 개의 탄소 중에서는 입체장애의 정도에 따라 상대적으로 입체장애가 작은 쪽의 원자에서 반응이 시작되는 경우가 많습니다.
일반적으로 경화를 시작하는 경우, 경화제 양을 에폭시 수지의 에폭시기에 대하여 반응기가 화학양론적으로 같은 몰 비로 되도록 정하는 것이 좋습니다. 예들 들면, 아민계 경화제를 사용한 경우에는, 몰 비를 에폭시기 : NH = 1:1, 산무수물계 경화제의 경우에는 에폭시기 : CO-O-CO = 2:1 로 혼합합니다. 그러나 가교반응이 일어나므로 반응의 후기에는 분자의 운동성이 억제되어 실제로 반응 속도가 크게 떨어지는 경우가 많기 때문에 실제 공정에서는 경화제를 약간 많이 사용하는 경우가 일반적입니다.
아민계 경화제의 기본적인 반응은 아래의 그림과 같이 진행되고, 가장 먼저 아민이 에폭시 고리에 붙습니다. 이 반응은 SN2형의 친핵성 치환반응이고, 반응계 중의 알코올성 OH기가 보조적으로 고리형성을 도와준다고 알려져 있습니다다.

Step 1 단계에서는 수지의 분자량이 증가함에 따라 점도가 높아지지만 gel화는 발생되지 않습니다. 이상적인 반응의 예지만, step1의 반응속도, 즉 제 1아민에서 제2아민을 생성하는 반응속도는 step2에서 제2아민에서 제3이만을 생성하는 반응속도의 약 2배 정도 높고 방향족 아민보다는 약 7~10배 높습니다. 따라서 반응을 일시적으로 step1에서 정지시킨 후 이어서 수지를 가열하여 step2의 반응을 진행하는 것이 가능하며 step 1에서 반응을 정지한 상태를 B stage라고 부릅니다. 에폭시 수지를 매트릭스로 하는 프리프레그 등의 성형재료의 제조공정에는 수지를 sheet상 또는 직물상의 강화용 수지에 함침시킨 후 가열하고 B stage 상태로 중지하여 만들게 됩니다. 수지 매트릭스를 B stage 상태로 존재하게 함으로써 실온에서 점착성을 갖고, 성형공정에서 적당한 유동성을 나타내는 성형재료가 얻어집니다.
산무수물의 반응은 촉매의 유무에 따라 달라지는데, 촉매인 제3아민이 존재할 경우에는 산무수물이 과잉으로 있기 때문에 평형이 우측으로 치우치면서 carboxyl anion을 생성합니다. 그리고 이 carboxyl anion은 에폭시기와 반응하여 alkoxy anion을 생성하고, 그 alkoxy anion이 다른 산무수물과 반응하여 다시 carboxyl anion을 생성하고 그 carboxyl anion이 같은 모양으로 에폭시기와 반응하여 경화 반응이 진행됩니다. 그리고 마지막으로 촉매는 떨어져 나오게 됩니다. 이러한 반응은 anion적인 교호반응이기 때문에, 일반적으로 ether 결합을 생성하지 않는다는 특징이 있습니다.
촉매가 존재하지 않는 경우에는, 에폭시 수지 중에 존재하는 OH기 또는 산무수물 중의 carboxyl기로부터 반응이 시작됩니다. 알코올성 OH기와 산무수물로부터 half-ether가 생성되고 여기서 생성된 carboxyl기가 에폭시기와 반응하고 ester화하여 알코올성 OH기가 생성됩니다. 같은 모양으로 이 알코올성 OH기와 산무수물로부터 half-ester를 생성하고, 여기서 생성된 carboxyl기가 다시 에폭시기와 반응하는 과정이 반복됩니다. 고상형의 에폭시 수지는 통상 액상 에폭시 수지와 비교해서 분자 내에 OH기를 많이 가지고 있기 때문에 경화 촉진제 없이도 경화가 진행되기는 하지만 경화 촉진제를 함유하는 액상 에폭시 수지에 비해 낮은 경화속도를 나타내기 때문에 높은 경화 온도가 필요합니다.
'재료공학' 카테고리의 다른 글
| 양극과 음극, Cathode와 Anode (4) | 2021.02.05 |
|---|---|
| 자기이방성 (0) | 2021.01.20 |
| 페리자성(Ferrimagnetism) (0) | 2020.12.14 |
| 유전율과 유전특성(dielectric property) (4) | 2020.09.10 |
| 물질의 물리적 성질에 대하여 (0) | 2020.08.07 |
댓글