불산이란 무엇인가?
작년 여름, 일본 정부가 대한민국을 상대로 반도체용 고순도 불산(플루오린화 수소, 불화수소)의 수출을 규제하여 큰 논란이 있었습니다. 반도체 공정에 반드시 필요한 물질이었는데 일본은 이를 무기삼아 한국을 때렸지만 생각만큼 한국이 타격을 입지 않았고 오히려 수입다변화와 국화를 촉진하게 되어 결과적으로는 실패한 규제가 되었습니다.

불산은 불화수소를 물에 녹인 약산 중 하나이며 불소의 높은 전기음성도로 인해 강한 수소결합을 형성하는 물질입니다. 이로 인해 물에 잘 용해되며 다른 할로겐화수소에 비해 녹는점과 끓는점이 높습니다. 실리콘이나 유리를 녹일 수 있어 여러 분야에서 널리 사용되지만 자극적인 냄새가 나며 반응성과 독성이 매우 큽니다. 강산으로 불리는 염산, 질산, 황산보다 산성도는 낮지만 훨씬 더 위험한 물질입니다. 저도 실리콘(Si)이나 반응성이 낮은 합금을 녹일 때 종종 사용했었는데 익히 불산의 위험성을 오래전부터 들었던 터라 온갖 종류의 안전보호구를 착용하고 긴장한 상태에서 실험을 했던 기억이 있습니다. 그렇다면 이제 왜 그토록 불산이 위험한지 그 이유에 대해 말씀드리겠습니다.
불산이 약산임에도 불구하고 강산보다 더 위험한 이유는?
약산이라는 것은 단순히 화학적으로 HF가 덜 해리된다는 뜻일 뿐 위험효과가 약하다는 뜻은 아닙니다. 사실 불산은 산성이라서 위험하기 보다는 ‘불소’의 높은 반응성으로 인해 인체에 치명적인 영향을 끼치는 것입니다.
우선 불산에 노출되게 되면 불소와 체내의 칼슘이 결합되어 신경기능이 손상되며 불소는 빠르게 체내의 뼈로 흡수되어 골밀도를 낮추어 골다공증이나 관절염을 일으킵니다. 대표적인 위험물로 알려진 황산과 비교를 한다면 아래와 같은 이유로 불산이 더 위험하다고 할 수 있습니다.
첫째, 불산에 의한 데미지는 즉각 관찰되지 않아서 위험합니다. 만약 진한 황산에 노출되었다고 하면 황산의 화학반응에 의해 노출 직후 강한 화학화상을 느낄 수 있습니다. 진한 황산에 노출되면 피부 표면에 하얀 물집이 잡힌 후 탄화되고 명백한 통증을 느낄 수 있기 때문에 이러한 통증이 환자를 최대한 빠르게 치료하게끔 만듭니다. 만약 진한 질산에 노출되었다고 해도 빠르게 물로 씻어낸다면 물집이 생기지 않으며 비교적 치료가 간단하고 큰 후유증이 남지 않습니다.
하지만 불산의 경우 30% 이상의 고농도 불산에 노출되는 경우에만 통증이 있고 낮은 농도(2%)의 불산에 노출되면 피부와의 반응에 의한 통증이 거의 없이 빠르게 신체 조직 내로 침투하여 치명적인 문제를 일으킵니다. 황산과는 달리 미량으로 노출된다 해도 반드시 피부 내로 침투하기 때문에 병원에서 전문적인 치료를 받아야 합니다. 더구나 황산은 점도가 높아 물과 구분하기 쉽지만 불산의 경우 물과 비슷하여 단순히 육안으로 구분하기도 어렵습니다.
둘째, 불산에 노출되게 되면 신체 여러기관에 광범위한 문제를 일으킵니다. 불산에 노출되면 빠르게 피부 아래로 스며들고 혈액에 섞여 전신 조직에 문제를 일으키는데 특히 뼈에 큰 문제를 일으킵니다. 불산과 칼슘이 만나 칼슘 이온을 불용성 불화칼슘으로 바꾸어 버리기 때문에 혈중 칼슘 농도가 급격히 저하하여 부정맥과 심장마비가 발생할 수 있습니다.
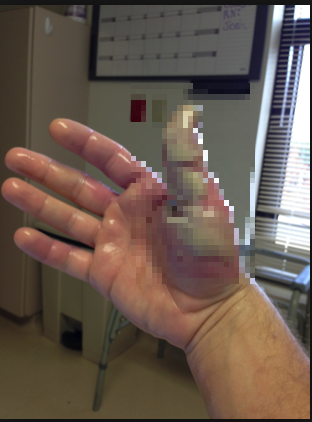
사실 불산이 정말 무서운 이유는 다른 곳이 있습니다. 차라리 심장마비로 사망하는 것이 축복일 정도입니다. 만약 불산이 체내로 들어와 손이나 발이 하얗게 변하게 된다면 절단하는 것이 가장 현명합니다. 이러한 상황이라면 조직 내에 많은 양의 불소 이온이 있다는 뜻인데 불소 이온은 체내 칼슘과 같은 금속 이온과 완전히 결합되지 않습니다. 세포가 사멸하는 과정에서 불소 이온이 계속 방출되며 다른 조직이 계속 불소 이온에 의해 공격당합니다. 노출량이 적은 경우 눈에 보이는 물집은 적지만 이런 불소 이온에 의해 손이나 발의 뼈에 점점 예리한 통증을 느끼게 됩니다. 나중에는 온 몸의 뼈에 심각한 통증이 발생하여 오랫동안 환자를 괴롭힙니다. 이와는 달리 황산이나 질산, 염산으로 인한 화학화상은 불산처럼 전신에 영향을 끼치지 않고 노출 부위에만 영향을 끼칩니다.

셋째, 치료 방법이 제한적이며 적절한 응급처치를 하여도 후유증이 남습니다. 만약 불산에 노출되었다면 칼슘 글루코네이트(Calcium gluconate, 상품명 칼고네이트 Calgonate)라는 연고 이외의 선택지가 없습니다. 국부적으로 효과가 있는 응급 치료제로 불산이 노출된 환부를 다량의 물로 깨끗이 씻은 후 넓게 연고를 바르면 됩니다. 이 연고를 바르게 되면 칼슘 글루코네이트가 불소이온과 결합하여 저칼슘혈증을 막아주지만 이 과정에서 많은 불용성 불화칼슘이 형성되어 신장에 문제를 일으킵니다. 많은 양의 불화칼슘이 형성된 경우 경우 전신에 결석이 생겨 엄청난 고통이 수반되는데 수술로 모두 제거하기가 쉽지 않습니다.
이토록 불산은 위험한 물질이며 노출 시 엄청나게 고통스러운 후유증으로 인해 극도로 주의해야 하는 물질입니다. 하지만 안타깝게도 지난 2012년 구미와 2013년 화성에서 불산 노출 사고가 발생하여 각각 5명과 1명이 사망하는 사고가 발생하였습니다.
만약 사고든 실수든 불산에 노출되게 된다면 최대한 빨리 비상샤워기로 달려가 모든 옷을 벗고 흐르는 물에 씻어내야 합니다. 그리고 칼슘 글루코네이트 연고를 바르고 지속적으로 문지르며 반드시 일반적인 화학 화상이 아닌 ‘불산’에 의한 화상임을 의료진에 전달해야 합니다. 만약 스스로의 힘으로 불산을 씻어내거나 칼슘 글루코네이트 연고를 바를 수 없다해도 주위에 안전한 보호구를 갖춘 사람에게만 도움을 요청해야 합니다. 또 주변에 불산에 노출된 환자가 있다 해도 안전한 보호구가 없다면 보호구를 착용하기 전까진 절대 섣불리 도와주지 않아야 합니다. 도움을 주는 사람도 같이 불산에 노출될 수 있기 때문입니다.
독극물 - 비소에서 복어독, 보톡스까지
독극물 - 비소에서 복어독, 보톡스까지 독극물이란? 독극물, 또는 독은 무엇일까요? 독극물의 과학적 정의는 ‘비교적 적은 양으로 유기체 내에서 기능장애를 일으키게 하는 물질'을 의미합니다. 여기서 ‘비교적..
luvlyday.tistory.com
강산(Strong acid)의 정의와 종류
강산의 정의와 종류 수용액 상에서 완전히 해리되거나 이온화 산을 강산이라고 합니다. 즉 효율적으로 양성자인 H+를 내어놓을 수 있는 화학물질이라는 뜻입니다. 강산은 수용액 안에서 양성자�
luvlyday.tistory.com
약산의 정의와 종류
약산의 정의와 종류 약산은 수용액에서 부분적으로 해리되는 산입니다. 이와 반대로, 강산은 물에서 완전히 해리되는 산을 의미합니다. 약산의 짝염기는 약염기이며 약염기의 짝산는 약산입니�
luvlyday.tistory.com
'화학' 카테고리의 다른 글
| [원자 구조] 원자 궤도(Orbit)와 오비탈(Orbital)의 이해 (0) | 2020.03.07 |
|---|---|
| 차아염소산나트륨(NaClO)의 특성과 사용법 (0) | 2020.03.04 |
| 독극물 - 비소에서 복어독, 보톡스까지 (0) | 2020.02.24 |
| [원자 구조] 원자 질량과 원자량의 기본 개념 (0) | 2020.02.18 |
| 과탄산소다(Sodium Percarbonate)의 특성과 용도 (0) | 2020.02.09 |

댓글