실리카(Silica, SiO2)란 무엇인가요?
실리카(Silica)는 이산화규소의 다른 말로, 화학식 SiO2를 가지는 물질을 뜻합니다. 지구상에서 가장 풍부한 원소인 실리콘(규소)과 산소가 결합하여 형성된 물질로, 모래나 여러가지 광물의 주요 성분으로 존재하고 지각을 이루는 화합물 중 가장 많은 비율을 차지합니다. 석영이나 유리, 흡습제인 실리카 겔을 구성하는 성분이기 때문에 우리주위에서 쉽게 찾아볼 수 있는 물질입니다.
실리카의 물리적, 화학적 성질
실리카의 분자량은 60.08이며 녹는점은 1743ºC, 끓는점은 2950ºC 입니다. 일반적인 상온, 대기압 조건에서 실리카는 고체 상태로 존재합니다. 실리카는 굉장히 다양한 결정구조를 가지며 각 결정구조마다 밀도나 열전도도, 색깔 등 여러가지 특성들이 조금씩 다릅니다.

실리카의 단결정 형태 중 하나인 석영을 구성하는 실리콘 원자는 사면체의 꼭지점을 둘러싸고 있는 산소원자와 공유결합을 이루고 있습니다
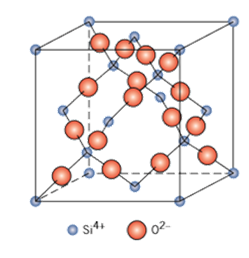
석영은 전기 저항과 유전강도가 높으며 특히 응력으로 인해 모양이 변하면 전압이 발생되는 압전특성을 가지고 있습니다. 또한 석영은 모스 굳기가 7에 이를정도로 단단하기도 합니다.
실리카를 이루는 화학결합의 극성은 거의 0에 가까운 안정적인 물질입니다. 결정성 실리카는 물이나 대부분의 산에 녹지 않지만 불산이나 뜨거운 수산화나트륨에는 녹습니다.
SiO2 + 6HF → H2SiF6 + 2H2O
SiO2 + 2NaOH → Na2SiO3 + H2O
또한 실리카의 용해도는 결정형태에 따라 차이가 있는데, 비정질 실리카의 용해도는 결정질 실리카인 석영의 용해도보다 서너배 가량 큽니다.

실리카의 용도
상업적인 실리카 생산량의 대부분은 모래 또는 콘크리트와 같은 건축재료로 사용되며 유리의 주요성분으로도 널리 사용됩니다.
실리카는 실리콘의 원료로도 사용됩니다. 실리카를 코크스(탄소)와 함께 가열하면 실리카가 환원되어 실리콘과 일산화탄소로 분해됩니다.
SiO2 +2C → Si + 2CO
실리카는 겔 형태로 가공되어 의약품이나 식품의 습도를 제어하는 흡습제로도 널리 사용됩니다.
실리카의 유해성
실리카는 화학적 반응성이 낮기 때문에 신체적 유해성 또한 높지 않습니다. 구강을 통한 섭취의 경우 반수치사량 LD50이 5g/kg 으로 낮지 않습니다. 오히려 하루 10 mg 정도의 소량의 실리카늘 섭취한 경우 치매의 위험이 약 11% 감소했다는 연구결과가 보고되었습니다.
구강을 통한 체내 흡수와는 달리, 호흡기를 통해 체내로 들어오는 실리카 분진은 여러가지 폐 질환의 원인이 될 수 있으니 주의해야합니다.
실리카겔(Silica gel)을 먹으면 어떻게 되나요?
실리카겔은 무엇인가요? 실리카겔은 화학식 SiO2인 이산화규소가 주성분인 물질로, 흡습제 또는 건조제로서 널리 사용됩니다. 조미김이나 육포같은 식품에서 새로 구매하는 신발 내부 등 일상상
luvlyday.tistory.com
'재료공학' 카테고리의 다른 글
| 그래핀(Graphene)에 대하여 (1) | 2020.05.29 |
|---|---|
| 탄소나노튜브(Carbon Nanotube, CNT)란 무엇인가 (1) | 2020.05.24 |
| 희토류(Rare Earth)의 성질과 용도 (0) | 2020.05.19 |
| 희토류(Rare Earth)의 종류와 뜻 (0) | 2020.05.19 |
| 실리콘(Silicon, 규소)이란 무엇인가? (1) | 2020.05.14 |

댓글